6月19日,国家药监局药审中心发布了《中国新药注册临床试验进展年度报告(2024年)》,透过这份厚重的年度报告,我们发现:细胞与基因治疗领域正以惊人的速度向前推进。
作为一直关注干细胞与基因疗法的读者,您是否也好奇:这一年,中国在这个前沿领域究竟有哪些新变化?哪些数据值得特别关注?今天,我们带你一一揭晓。
细胞与基因治疗:增速最快的“新宠”
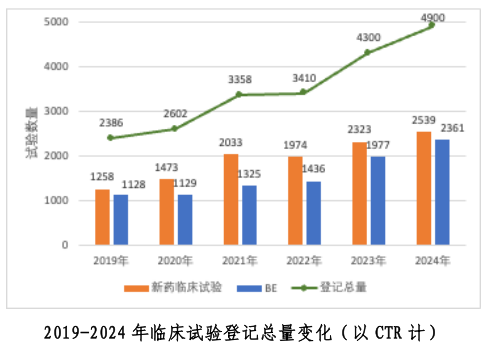
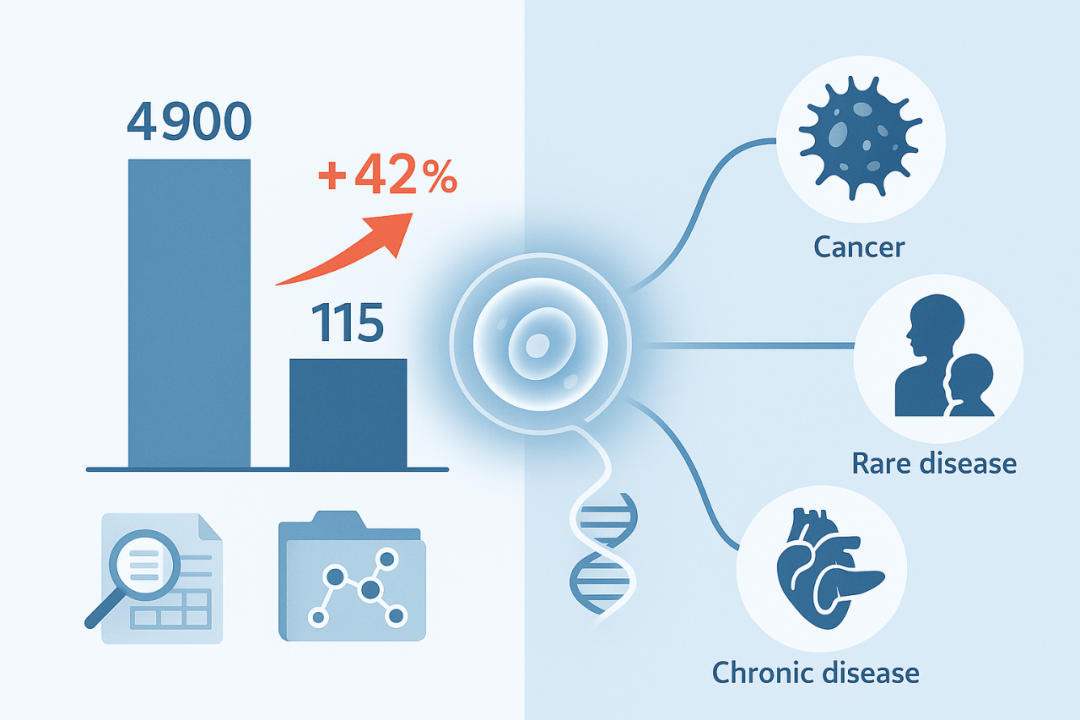
2024年,中国全年首次登记的新药临床试验达4900项,其中细胞与基因治疗相关试验共115项,同比增长42%,成为增长速度最快的赛道。
究竟是什么让这个领域如此火热?答案并不复杂:细胞与基因疗法代表着医学未来的无限可能。肿瘤治疗、罕见病康复、慢病管理,这些领域的突破性进展都离不开细胞和基因治疗技术的加持。
赛道分布:细胞疗法与基因疗法并行
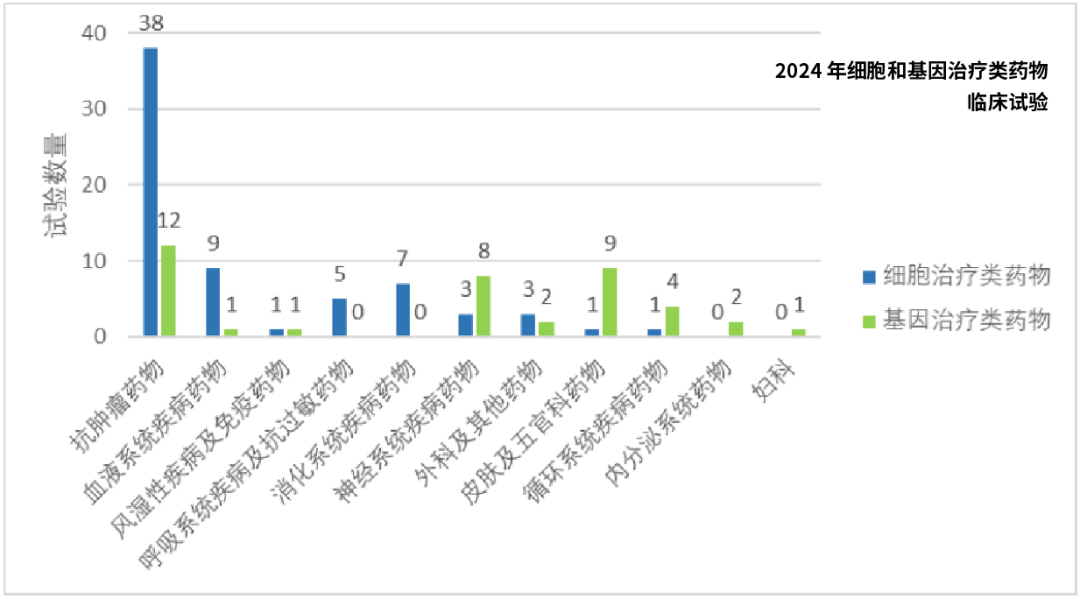
2024年,共计有100个细胞和基因治疗产品进入临床研究阶段,其中62个为细胞治疗产品,38个为基因治疗产品。细胞疗法更受企业青睐,占总量约62%,体现出行业对细胞治疗临床转化的积极性。
具体来看:
干细胞疗法最受关注,占全部试验的25.2%;
CAR-T细胞疗法紧随其后,占23.5%;
新兴的溶瘤病毒和TIL(肿瘤浸润淋巴细胞)分别占7.0%和5.2%。
值得一提的是,干细胞疗法全部聚焦在非肿瘤领域,如血液系统、消化系统和呼吸系统疾病治疗,凸显了干细胞广泛的应用潜力与普适性。
临床试验进程:I期为主,上市III期仍需突破
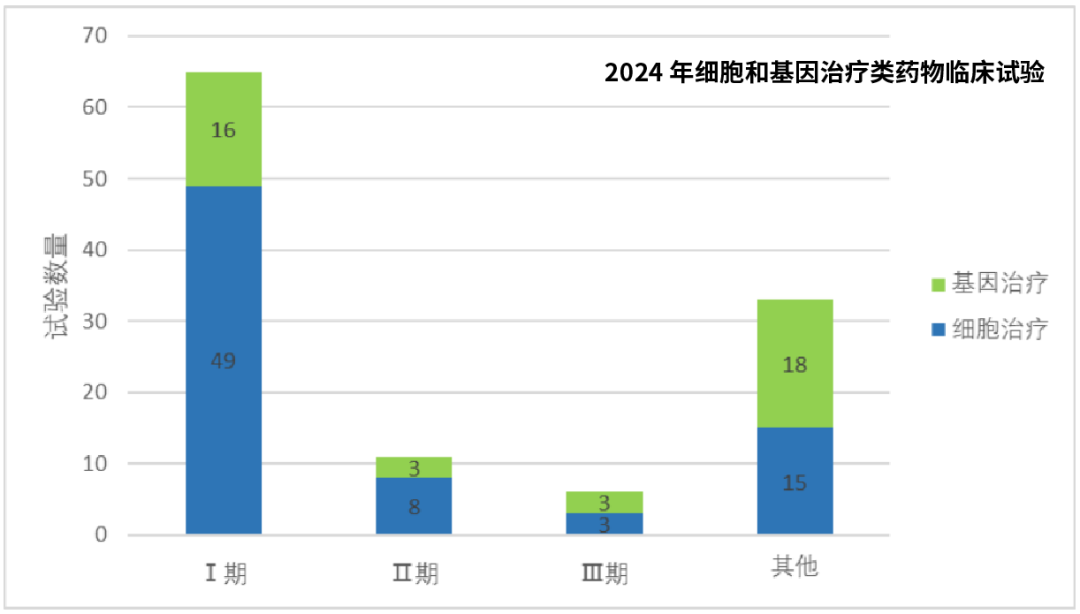
虽然整体数量增长迅猛,但从临床试验分期来看,中国细胞与基因治疗领域仍处于初步探索阶段:
I期临床试验占比高达56.5%,仍以安全性和初步疗效为主;
II期试验占比不足10%,III期更是稀少,仅占5.2%。
这也提示我们,尽管前景无限,真正迈向市场、惠及大众患者的成熟产品依旧稀缺。
干细胞项目特写:间充质干细胞(MSC)领跑
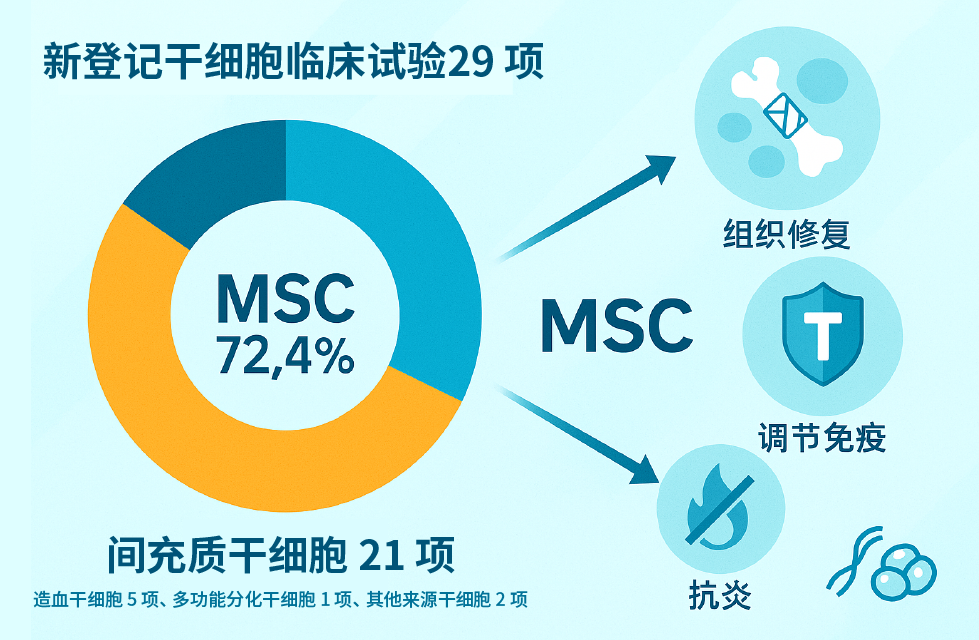
2024年共有29项干细胞临床试验新登记,从细胞来源来看中间充质干细胞(MSC)21项占据绝对主力,高达72.4%,在修复组织损伤、抗炎、调节免疫功能等方面展现出卓越的潜力。
间充质干细胞因其来源广泛、免疫原性低,成为企业布局的重点。但需注意的是,虽然潜力巨大,真正进入III期、即将冲击上市的干细胞疗法仍屈指可数。
审评审批提速:从批准到首例入组仅需6个月?
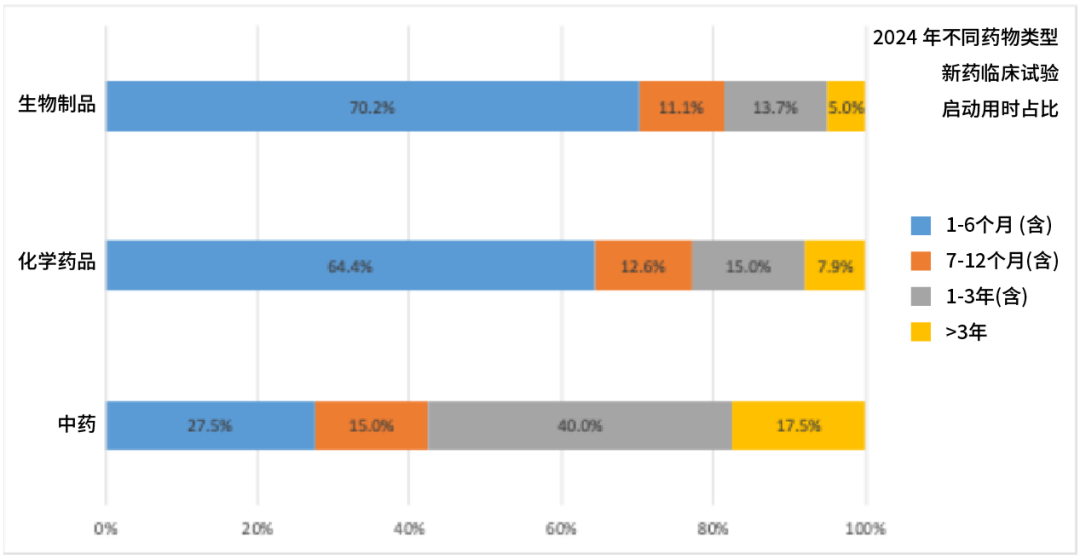
报告中另一个值得关注的趋势是审评审批效率的显著提高。65.5%的细胞与基因治疗项目,从获批到首例受试者入组只需不到6个月。
速度加快,意味着患者可以更快接触到前沿疗法,但监管部门和企业的责任也更加重大:疗效与安全必须同时兼顾,不能因为快而降低标准。
2025年展望:市场成熟度与患者可及性成为焦点
展望未来,我们认为以下几个趋势将在2025年及以后格外重要:
III期临床破局:谁将率先完成大规模III期试验,实现商业化落地?这是明年最值得期待的看点。
差异化竞争格局形成:CAR-T疗法逐渐进入红海,溶瘤病毒、mRNA基因编辑技术或成新的风口。
医保与商业支付:细胞基因治疗价格昂贵,未来如何通过医保、商业保险及患者援助方案提高可及性,将是决定市场规模的重要因素。